Eruvchanlik - bu moddaning suvda yoki boshqa erituvchida erishi. Ham qattiq, ham suyuq va gazsimon moddalar suvda erishi mumkin. Eruvchanligi bo'yicha barcha moddalar uch guruhga bo'linadi:
- juda eriydi
- ozgina eriydi
- erimaydigan
Mutlaqo erimaydigan moddalar mavjud emas, shuning uchun erimaydigan ism shartli va siz "amalda erimaydigan" narsani o'qishingiz kerak.
Moddaning eruvchanligi haroratga bog'liq, masalan, haroratga va bosimga bog'liq, masalan, KNO moddasi3 (kaliy nitrat) + 20 ° C haroratda 31,6 g / 100 g suvda eriydi va + 100 ° C haroratda - 245 g / 100 g suv.
Oddiy sharoitlarda tuzlarning eruvchanligi, yog'ingarchilik va gidrolizlanishi

Jadval uchun tushuntirishlar:
- P - tuz eriydi (0,1 mol / l dan ortiq),
- M - kam eriydigan tuz (0,1-0,001 mol / l),
- N - erimaydigan tuz (0,001 mol / l dan kam),
- [N] - qaytarilmaydigan gidroliz, tuz eritmadan cho'kmaydi, asosiy tuz karbonat angidrid ajralib chiqishi natijasida hosil bo'ladi, Cr2S3 - Cr (OH) cho'kindi3 vodorod sulfidi ajralib chiqishi bilan
- + - tuz suv bilan to'liq reaksiyaga kirishadi,
- - - mavjud emas,
- * P - kation bilan gidrolizlanadi,
- P * - anion gidrolizlanadi.
Tuzlarning eruvchanligi
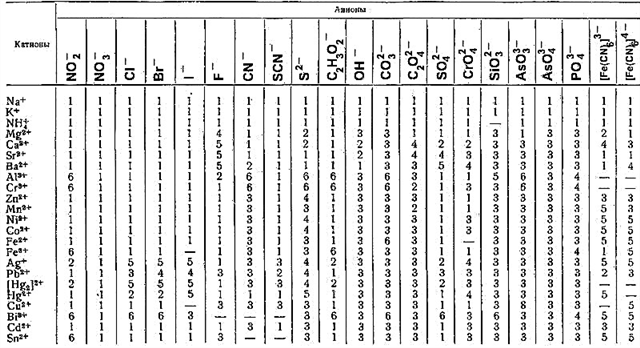
Jadval uchun tushuntirishlar
- 1 - tuz suvda eriydi,
- 2 - suvda ozgina eriydi,
- 3 - suvda erimaydigan, ammo organik va mineral kislotalarda eriydi,
- 4 - suvda va organik kislotalarda erimaydigan, ammo mineral kislotalarda eriydi,
- 5 - tuz suvda ham, kislotada ham erimaydi,
- 6 - gidrolizlangan.
Agar sizga sayt yoqqan bo'lsa, biz uni ommalashtirishdan minnatdormiz :) Do'stlaringizga forumda, blogda, hamjamiyatda ayting. Bu bizning tugmachamiz:
Tugma kodi: